Главные события в биофармацевтике в 2024 году

Прорывные исследования, новые стандарты терапии и законодательные решения формируют тренды в фармацевтической отрасли и медицине на ближайшие годы. Расскажем, что важного произошло в биофармацевтике в 2024 году.
Этот материал мы подготовили по итогам доклада директора Научного центра трансляционной медицины Университета «Сириус» Романа Иванова, с которым он выступил на саммите Сириус.БИОТЕХ 2025.
Checkpoint-ингибиторы
Главным событием в области онкологии в прошлом году стало появление новых эффективных препаратов для иммунотерапии рака. В течение последних 10 лет сотни компаний искали комбинированные подходы к терапии онкологических заболеваний с целью увеличить эффективность checkpoint-ингибиторов. Почти все попытки заканчивались неудачей, пока в 2024 году китайская компания Akeso не представила результаты клинического исследования биспецифических антител, которое сочетает в себе checkpoint-ингибитор анти-PD-L1 и способность ингибировать (замедлять) фактор роста эндотелия сосудов VEGF. Антитела против VEGF имеют синергию с checkpoint-ингибиторами, но такая комбинация двух отдельных лекарств приводит к увеличению частоты и тяжести побочных эффектов. Комбинирование этих двух механизмов в одной молекуле биспецифического антитела показало хороший результат в борьбе с опухолями.
Китай сегодня — кузница лекарств для лечения онкологических больных
Роман Иванов
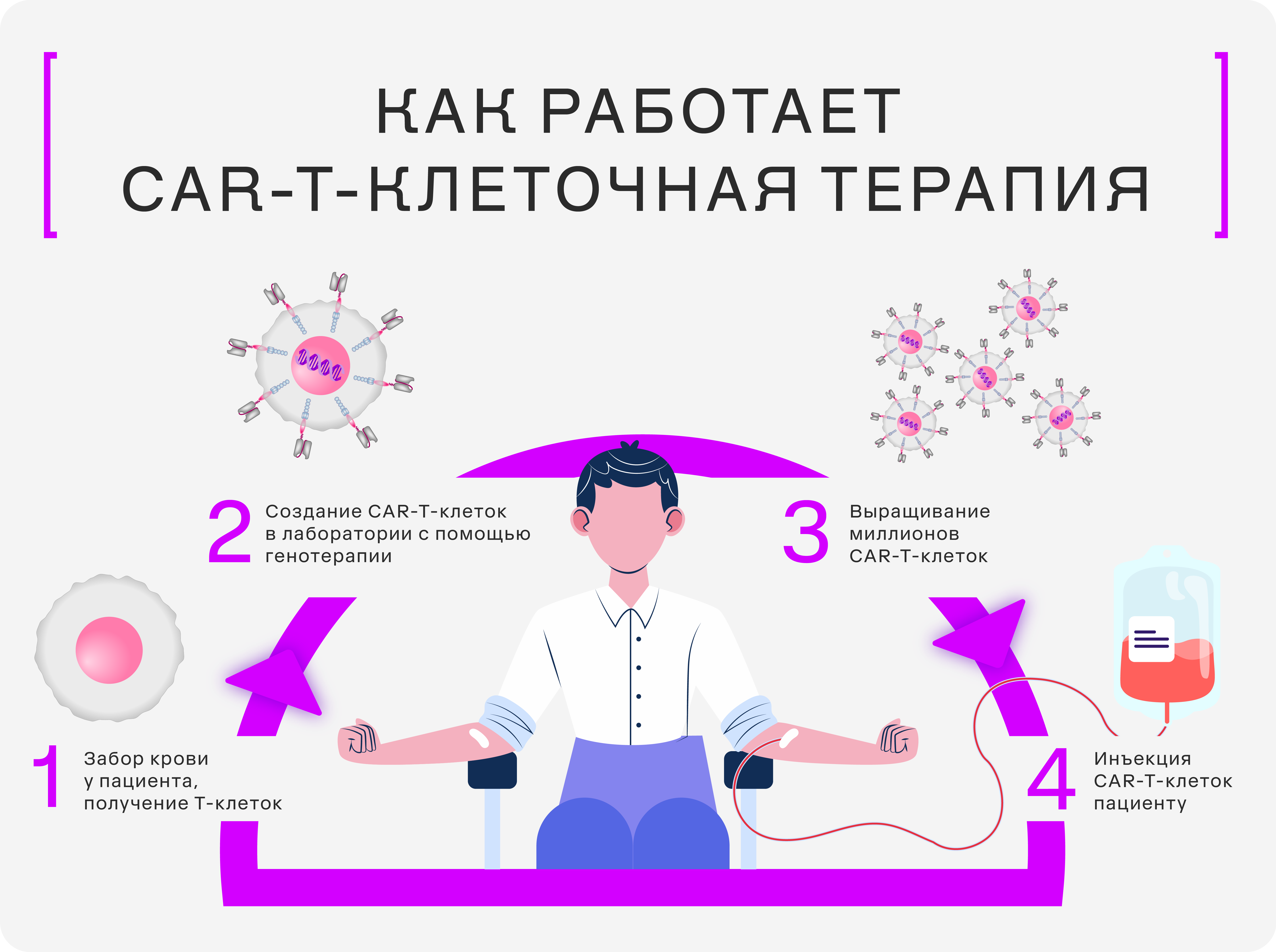
CAR-T-терапия
CAR-T-терапия показала превосходный результат в исследованиях прошлых лет и сегодня является одним из эффективных методов лечения онкогематологических заболеваний (лейкозов и лимфом). До недавнего времени не удавалось продемонстрировать эффективность этого подхода при других типах опухолей из-за иммуносупрессивного микроокружения, которое мешает работе иммунной системы. В Китае впервые показали эффективность CAR-T-терапии в борьбе с раком печени — заболеванием, которое очень тяжело поддаётся лечению. Благодаря генетическим модификациям Т-лимфоцитов учёным удалось преодолеть иммуносупрессивное микроокружение опухоли и добиться первого убедительного успеха в терапии рака печени; также в прошлом году была показана эффективность этого подхода в лечении опухолей желудочно-кишечного тракта, а также глиобластомы.
Главный тренд последнего времени в CAR-T-терапии — массовое движение в сторону in vivo CAR-T подходов. Стандартная CAR-T-терапия — это сложный и дорогостоящий процесс, для которого необходима современная лабораторная и производственная инфраструктура. Благодаря технологии липидных наночастиц учёные смогли вводить кодируемые молекулами РНК химерные антигенные рецепторы в кровоток пациента, превращая клетки иммунной системы в CAR-Т-лимфоциты, которые обнаруживают и уничтожают опухоль. Технология была успешно применена для лечения диффузной В-крупноклеточной лимфомы — через месяц после начала терапии наступила полная ремиссия.
«Сейчас наши коллеги из КНР и Европы начали клинические исследования аналогичного подхода для лечения множественной миеломы. Западные компании пытаются догнать китайских коллег, начиная исследования CAR-Т-терапии, а также введения химерных антигенных рецепторов в фагоцитирующие клетки, нацеливая клетки врождённой иммунной системы на опухолевые антигены. У нас в Университете „Сириус“ в прошлом году начат проект по созданию платформы in vivo CAR-T с использованием липидных наночастиц», — говорит Роман Иванов.
Генная терапия
2024 год отметился прорывными результатами лечения наследственной глухоты. Отличились в этом и китайцы, и американцы. Технология доставки белка отоферлина с помощью двух аденоассоциированных вирусных векторов продемонстрировала эффективность. Меньше месяца назад в США одобрен для использования один из первых препаратов для лечения буллёзного эпидермолиза. Это лекарство основано на генетически модифицированных аутологичных клетках, в которых при помощи вектора компенсирован генетический дефект синтеза коллагена, приводящий к развитию врождённого заболевания.
 Буллёзный эпидермолиз является результатом мутаций в более чем 10 генах
Фото: © janith priyasanka / Shutterstock / FOTODOM
Буллёзный эпидермолиз является результатом мутаций в более чем 10 генах
Фото: © janith priyasanka / Shutterstock / FOTODOM
Что такое буллёзный эпидермолиз?
Буллёзный эпидермолиз — наследственное заболевание, характерными симптомами которого являются волдыри на коже, которые могут возникать из-за травм или даже прикосновений. В случае буллёзного эпидермолиза мутации в генах вызывают нарушения в структуре белков, отвечающих за соединение между эпидермисом и дермой. В результате эти белки не могут нормально функционировать и поддерживать правильное положение и близость слоев кожи, что делает её более уязвимой.
Основная задача такой терапии — модифицировать геном культивируемых фибробластов пациента и нарастить их в достаточном количестве. Важно объединить эти два процесса и создать продукт, который представляет собой лоскутки генетически модифицированной кожи, которую трансплантируют пациенту для заживления ран. В итоге этого удалось добиться.
Главный прорыв прошлого года — in vivo генная терапия с помощью инструментов редактирования генома. Речь идёт о лечении наследственного ангионевротического отёка — орфанного заболевания, которое проявляется в виде внезапных болезненных отёков. В печень пациента с такой патологией с помощью липидных наночастиц была доставлена система CRISPR-Cas, которая нокаутировала (выключила) ген прекалликреина (отвечает за воспаление), снизив уровень белка и практически полностью избавив больного от приступов.
Учёные Университета «Сириус» сейчас работают над проектами, связанными с in vivo доставкой инструментов редактирования генома для лечения ретинопатии, а также гемофилии.

Способ избавить детей от слепоты нашли ученые «Сириуса»
ЧитатьМезенхимальные стволовые клетки
В 2024 году первый успех был у препарата на основе мезенхимальных стволовых клеток [клетки, которые способны превращаться в клетки разных тканей организма] для терапии реакции «трансплантат против хозяина» [побочный эффект, который может развиваться после пересадки стволовых клеток или костного мозга, когда клетки иммунитета воспринимают донорские клетки как патоген] после трансплантации стволовых клеток. Первое лекарство, одобренное в США для борьбы с подобной реакцией, называется Рионцил. Мезенхимальные клетки для этого лекарства получают из костного мозга здоровых взрослых людей-доноров.
Редактирование мРНК и мРНК-препараты
Прошлый год ознаменовался первыми результатами клинического применения технологии редактирования матричной рибонуклеиновой кислоты. Такой подход хорош тем, что обходится без вмешательства в геном (это безопасно и имеет обратимый эффект) и хорошо зарекомендовал себя при дефиците альфа -1- антитрипсиновой недостаточности, гемофилии и молекулярной дегенерации. Китайские учёные создали уникальную панель инструментов редактирования ДНК и РНК, использовав результаты своих исследований для лечения наследственных патологий мозга и других орфанных заболеваний.

Болезни-«сироты»: можно ли вылечить от редких недугов?
Читать«Хочется сказать и об успехах применения мРНК-препаратов, а также препаратов на основе кольцевой мРНК, которые изучаются в нашем Университете. В этом году первый такой препарат дошёл до стадии клинических исследований. Он предназначен для онкопациентов, которые испытывают неприятную сухость во рту из-за лучевой терапии. С помощью молекул кольцевой РНК это средство доставляет ген, который увеличивает образование слюны и улучшает качество жизни пациентов», — отмечает Роман Иванов.

Зачем магистрант «Сириуса» разрабатывает искусственную слюну
ЧитатьПочему китайцы успешны в фармацевтике?
Компании из КНР преуспевают на рынке фармацевтических препаратов благодаря сочетанию государственной поддержки инноваций с грамотной кадровой политикой и снижению административных барьеров для внедрения в практику результатов научных исследований. В Китае существует особая процедура одобрения инициативных клинических исследований ( investigator-initiated studies), которые учёные в университетских клиниках могут проводить без получения стандартного разрешения на клинические исследования.
Эпигенетическое редактирование
Другое событие прошедшего года — начало исследований в области эпигенетического редактирования с помощью фермента нуклеазы, которая сшита с метилтрансферазой и может прицельно влиять на метилирование определённых генов, выключая их экспрессию. Эпигенетическое редактирование показало эффективность при лечении хронического гепатита В. Также изучаются способы выключения генов, отвечающих за сенесцентный фенотип клеток, предотвращая их старение.
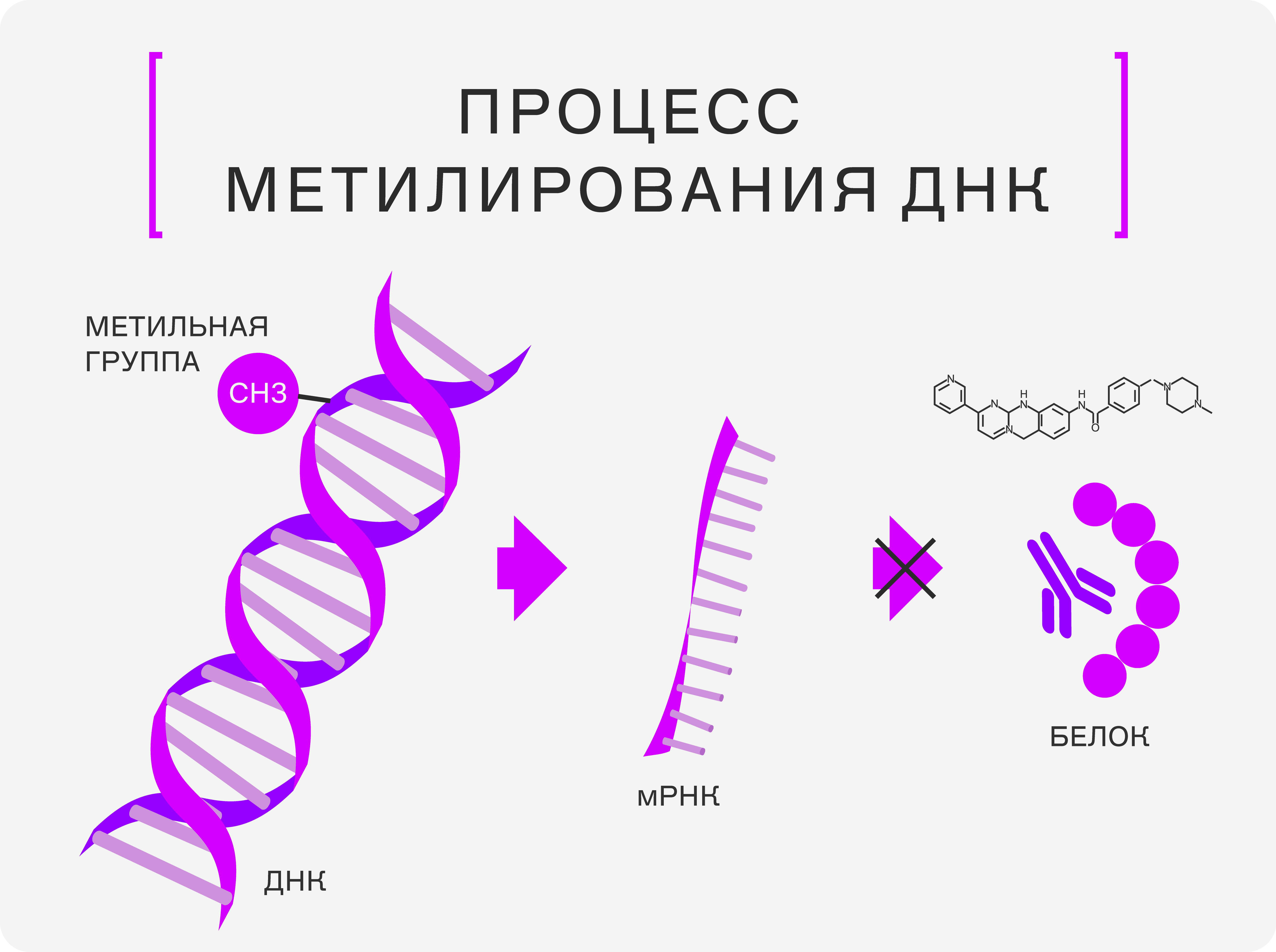 К нити ДНК присоединяется метильная группа (CH3), и на основе ДНК синтезируется мРНК. Если метильная группа расположена на нуклеотиде, который служит началом для считывания информации, то ген может "выключаться" и белок не будет синтезироваться
Изображение: © Яна Алябьева / «Сириус(Журнал»
К нити ДНК присоединяется метильная группа (CH3), и на основе ДНК синтезируется мРНК. Если метильная группа расположена на нуклеотиде, который служит началом для считывания информации, то ген может "выключаться" и белок не будет синтезироваться
Изображение: © Яна Алябьева / «Сириус(Журнал»
Терапевтические олигонуклеотиды
Терапевтические олигонуклеотиды — это препараты на основе короткой (15–25 нуклеотидов) последовательности ДНК или РНК. Долгое время они были на периферии внимания разработчиков лекарств, но в последние годы ими стали заниматься активнее. И вот американская компания Eli Lilly опубликовала результаты исследований липодисирана — малой интерферирующей РНК, которая ингибирует синтез липопротеина А. Благодаря этому препарату уровень липопротеина снижался почти до нуля, что важно для профилактики сердечно-сосудистых заболеваний.