Евгений Рогаев — о первом мозге, бессмертной медузе и лекарстве от Альцгеймера

В нашей стране он был пионером внедрения методов ДНК-идентификации в криминалистике и анализе отцовства, а также в поиске неизвестных генов наследственных болезней. Евгений Рогаев — выдающийся российский учёный, который сегодня трудится и преподаёт в Университете «Сириус». Мы поговорили с ним о том, как его любимая генетика изменила подход к научным исследованиям в России, можно ли обезопасить ребёнка от болезни Альцгеймера и защитить диссертацию без научрука.
Мы продолжаем серию интервью с российскими учёными, у которых накоплен опыт работы за рубежом, у многих — весьма солидный. Им есть с чем сравнивать, поэтому говорим с ними не только о профильных исследованиях, но и о том, как развивается наука в России и других странах.
— Евгений Иванович, вы занимаетесь поиском генов, связанных с различными заболеваниями. Как вы оказались в США для изучения болезни Альцгеймера?
— Во второй половине 1980-х годов в Советский Союз приехал учёный и врач Дэниел Поллен. Вместе с учёными из Гарвардского университета он начинал заниматься генетикой болезни Альцгеймера. Про гены этого недуга в то время ничего не было известно. На первом этапе надо было собрать семьи, у членов которых такая патология встречается часто, а значит, имеет наследственную природу. С появлением особого подхода, названного генетическим сцеплением, учёные (их даже стали называть «охотники за генами») принялись искать гены, мутации в которых приводят к наследственным заболеваниям (как правило, врождённым).
В одной из родословных, собранных Полленом, значились литовские евреи. Тогда он приехал в СССР искать эти корни, но, кажется, не нашёл. Зато впоследствии написал книгу, в которой рассказал, как всё начиналось, как познакомился со мной и как дальше развивалась история поиска генов болезни Альцгеймера.
 Книга Дэниела Поллена «Наследники Ханны: в поисках генетического происхождения болезни Альцгеймера» вышла в 1996 году
Изображение: © Яна Алябьева / «Сириус(Журнал»
Книга Дэниела Поллена «Наследники Ханны: в поисках генетического происхождения болезни Альцгеймера» вышла в 1996 году
Изображение: © Яна Алябьева / «Сириус(Журнал»
Дело в том, что для генетического сцепления необходимы маркеры ДНК, покрывающие геном. Они позволяют отслеживать сцепку определённых участков хромосом с конкретными болезнями. В то время этих маркеров было не много, но у меня такие были, ведь я тогда активно занимался геномикой. Учёные из Гарвардского университета начали проводить исследования по генетическому сцеплению нейродегенеративных заболеваний и пригласили меня к себе в лабораторию. Я съездил на несколько месяцев.
Кто такой Евгений Рогаев?
Евгений Рогаев — доктор биологических наук, специалист в области молекулярной генетики, нейрогенетики, эволюционной геномики. Академик РАН и лауреат Государственных премий РФ в области науки и техники (в 1996 и 2017 годах).
— Почему решили уехать?
— Я планировал поездку на небольшой срок, ведь в СССР у меня была своя лаборатория — в Научном центре психического здоровья РАМН. Потом Советский Союз распался, а учёные, с которыми я работал в Гарварде, уехали заниматься наукой в Канаду (на руках у них уже были родословные людей со всего мира, страдавших болезнью Альцгеймера). Они пригласили меня продолжить исследования там, и я согласился, но с сохранением лаборатории в России.
Тогда шла настоящая охота за генами, и мы в итоге первыми нашли тот, что отвечает за развитие болезни Альцгеймера
Вообще, считалось практически невозможным сделать это с помощью методов генетического сцепления, которые мы использовали. Дело в том, что они основаны на анализе родословной, где отмечаются больные и здоровые члены семьи. Для этого берётся образец ДНК, определяются хромосомы и распределённые вдоль них различные маркеры. Учёные прослеживают, как последние передаются из поколения в поколение. Если конкретный маркер наследуется одновременно с заболеванием, значит, ген, ответственный за эту патологию, расположен недалеко от него на хромосоме.
Но с болезнью Альцгеймера всё сложнее. Она же не врождённая, поэтому непонятно, можно ли отнести, например, 60-летнего испытуемого к здоровым. Или он больной, но симптомы у него ещё не проявились. Кроме того, считалось, что болезнь обусловлена несколькими факторами, а не одним геном.
— И врачи до сих пор не научились лечить болезнь Альцгеймера…
— Обычно учёные ищут гены болезней (точнее, гены с мутациями, которые приводят к болезням) для диагностики или выявления потенциальной мишени для терапии как первопричины недуга. История с болезнью Альцгеймера такова, что мы нашли гены и знаем теперь её молекулярный механизм, но это не помогло создать лекарство, которое было бы эффективно в клинических испытаниях, а не просто на модельных животных. Пока результата нет, но мы не опускаем руки. Сейчас ищем протектирующие факторы, то есть вещества или условия, которые помогают замедлить или предотвратить развитие заболевания.
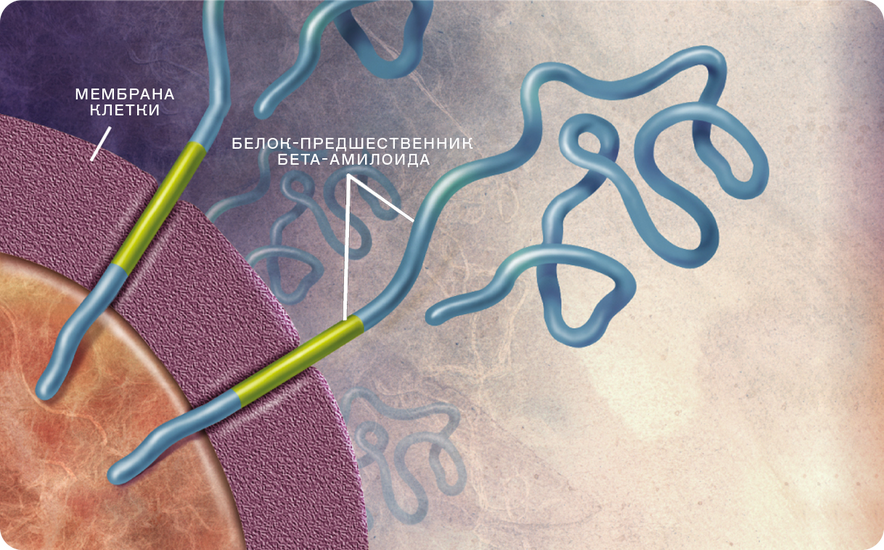
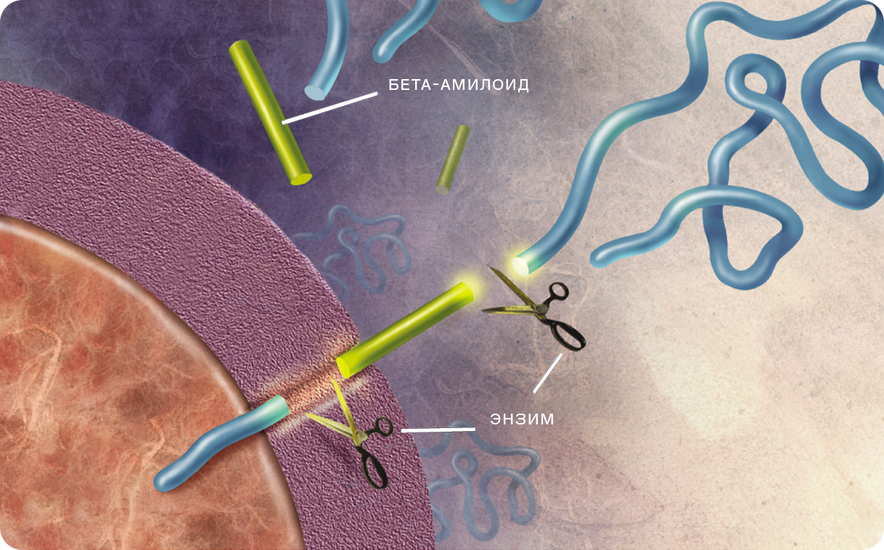
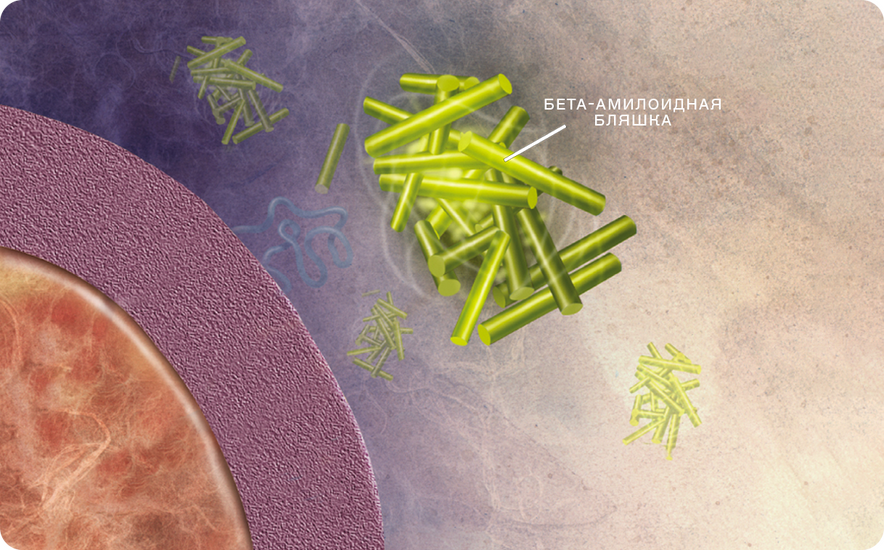
Мы знаем теперь гены (гены пресенилинов), мутации в которых ведут к ранней болезни Альцгеймера. Есть случаи, в которых возникают мутации в гене амилоидного предшественника. Пресенилины оказались необычными ферментами, которые расщепляют амилоидный предшественник, из-за чего образуется белок. Он накапливается в мозге — и формируются амилоидные бляшки, что приводит к дегенерации участков головного органа, связанных с памятью.
Существуют и так называемые генетические факторы риска, которые, повышают вероятность развития патологии. Например, генетический вариант е4 в гене АpоЕ, который кодирует белок, необходимый для транспортировки липидов. У его носителей риск заболеть выше, чем у остальных людей.
 Сравнение здорового мозга с мозгом, поражённым болезнью Альцгеймера
Изображение: © Яна Алябьева / «Сириус(Журнал»
Сравнение здорового мозга с мозгом, поражённым болезнью Альцгеймера
Изображение: © Яна Алябьева / «Сириус(Журнал»
Симптомы ранних форм болезни Альцгеймера могут проявляться уже с 40 лет. Это часто связано с мутациями в генах пресенилинов и амилоидного предшественника. К 65 годам у большинства людей с такими мутациями развиваются когнитивные нарушения. Для более распространённых поздних форм характерно присутствие е4. Но болезнь может возникнуть и без этих генетических факторов.
Именно обнаружение генетических мутаций позволило раскрыть механизм развития болезни Альцгеймера. Теперь мы понимаем, как она возникает. Независимо от того, есть мутации в этих генах или нет. Ключевой процесс один — необычные ферменты пресенилины способны разрезать белки внутри клеточной мембраны и расщеплять амилоидный предшественник. Обнаружение пресенилиров важно не только для изучения болезни Альцгеймера. Оно показало, что в клетках существуют необычные ферменты, разрезающие другие белки внутри клеточных мембран, за счёт чего осуществляется контроль многих биологических процессов. Идеально было бы воздействовать именно на этот механизм как первопричину болезни.
— Есть ли какая-то профилактика генетических форм болезни Альцгеймера?
— Для некоторых случаев мы знаем точно до клинического проявления, что болезнь обязательно разовьётся. Например, для аутосомно-доминантного заболевания, когда мутация присутствует только в одной копии гена, полученной от одного из родителей. Именно к таким формам относится болезнь Альцгеймера с мутациями в генах пресенилинов или амилоидного предшественника.
 Около 60 млн человек во всем мире страдают деменцией, наиболее распространенной ее формой считается болезнь Альцгеймера, она может быть причиной 60–70 % случаев
Фото: © illustrissima / Shutterstock / FOTODOM
Около 60 млн человек во всем мире страдают деменцией, наиболее распространенной ее формой считается болезнь Альцгеймера, она может быть причиной 60–70 % случаев
Фото: © illustrissima / Shutterstock / FOTODOM
Для этого нужна доклиническая диагностика. Известен случай, когда женщина обратилась в клинику, обеспокоенная риском развития болезни Альцгеймера у её будущих детей. В семье уже были случаи этого недуга, и обследование подтвердило наличие мутации в соответствующем гене. Чтобы избежать передачи будущему ребёнку, врачи отобрали яйцеклетки без мутации и провели процедуру искусственного оплодотворения. Такой подход обычно применяется для предотвращения врождённых заболеваний.
Значит, можно «создать» здорового ребёнка, выбрав яйцеклетку без мутации
Но в случае с Альцгеймером возникает этический вопрос: оправданно ли применение подобных методов для заболеваний, которые могут проявиться только в позднем возрасте?
Что касается существующих лекарств против этой болезни, то они обычно оказываются неэффективными на той или иной стадии клинических испытаний. Одно из возможных объяснений — испытания проводятся на пациентах уже после начала у них дегенеративных процессов. Возможно, следует проводить такие исследования на людях, которые находятся в группе высокого генетического риска, но ещё не заболели.
— Вы ещё нашли ген катаракты и облысения. И вообще у вас очень солидный послужной список. А с чего всё началось? Как вы пришли в науку? И почему именно биология? Откуда вы родом?
— Я родился в сибирской тайге — в Кемеровской области. Там были лесозаготовки и небольшая деревня. Река, ягоды, комары, медведи — настоящий рай! (Улыбается.) Родители были учителями, и семья переезжала, так что до 12 лет я жил в деревне на Алтае, на берегу реки Обь. Потом мы перебрались в Мариуполь, тогда он назывался Жданов, жили рядом с морем.
Меня всегда интересовало всё живое — и на воде и на суше: потрясающее многообразие и устройство животного мира. Я читал журналы «Юный натуралист», «В мире животных», «Наука и жизнь», а также известных писателей: Джеральда Даррелла, Яна Линдблада, Конрада Лоренца. Школу окончил в Мариуполе, после чего поступил в МГУ и занялся наукой.
— Наверное, трудно было поступить в один из главных вузов страны…
— Для того чтобы заниматься наукой, нужно было идти либо в Московский университет, либо в Ленинградский. Остальные, как считалось, выпускали преподавателей. В МГУ был огромный конкурс, и мне говорили, что шанс поступить очень низкий. Но я поступил и в итоге окончил кафедру генетики.
— Что для себя вынесли из учебы в университете?
— Я убежден, что знания человек получает главным образом через самообразование. Если у него нет стремления самостоятельно учиться, никакие внешние стимулы не помогут. Московский государственный университет даёт большие возможности по взаимодействию с научно-исследовательскими институтами. Большинство студентов пишут дипломы и курсовые работы именно в таких учреждениях. Пожалуй, это прямой путь в науку. Важно попасть в нужное место и суметь реализовать себя, что у меня и получилось. Диплом я писал в Научном центре психического здоровья РАМН, где начал заниматься генетикой человека.
Правда, когда я пришёл в лабораторию, это была пустая комната, в ней даже столов не было
— И что вы там делали?
— Начал с нуля — принялся конструировать лабораторные столы из детской финской мебели и собирать первые приборы. Зато там были сильные молодые энтузиасты, способные технически изобретать то, что в то время нельзя было достать или купить в СССР. Именно в этой лаборатории мы начали развивать первые методы секвенирования особых повторяющихся компонентов генома человека. Приборы для этого делали из стеклянных полок, которые приехали вместе с мебелью и оказались удивительно термостойкими. Работа в то время была основана на использовании радиоактивных изотопов в постоянном и активном режимах. Сейчас используются безвредные для здоровья флуоресцентные метки. Нашей первоначальной целью было выявить ген сложного психического заболевания — шизофрении. Эта задача остаётся актуальной до сих пор.
 Здание МГУ на фотографии 1983 года, когда этот университет окончил Евгений Рогаев
Фото: © Виктор Кошевой / ТАСС
Здание МГУ на фотографии 1983 года, когда этот университет окончил Евгений Рогаев
Фото: © Виктор Кошевой / ТАСС
— Как началась работа по ДНК-идентификациям? Как вы попали в криминалистику?
В 1988 году я защищал диссертацию без научного руководителя, и это было настоящей борьбой
Тема моей кандидатской касалась обнаружения гипервариабельных элементов генома. Оказалось, что в ДНК существуют разные повторяющиеся структуры, по которым люди сильно отличаются друг от друга. Сегодня всё это очевидно, но тогда было неизвестно. Так случилось, что де-факто я был без руководителя на защите. Обсуждение в Медико-генетическом институте было бурным.
Докторскую я защитил в 1996 году — удалось выявить ещё некоторые полиморфные маркеры для идентификации людей и животных. Пока я изучал свои варианты гипервариабельных повторов ДНК, в журнале Nature появились данные британского генетика Алека Джеффриса о других высокоинформативных семействах повторов ДНК, на основе которых можно получить индивидуальный профиль человека.
Что касается криминалистики, мы связались с судмедэкспертами, чтобы предложить им апробировать новый метод распознавания преступников на основе генетических материалов. Там посмеялись и сказали, что способ идентификации по группе крови ничто и никогда не заменит. Но в 1986–1988 годах я применил этот подход для определения отцовства, а также в криминалистике. Тогда же была запущена и Всесоюзная программа по разработке и освоению методологий совместно с Центром криминалистики МВД. В моей генетической лаборатории новые методики изучали сотрудники министерства в чинах майоров и капитанов. Мы разрабатывали подходы и тестировали объекты, из которых можно извлечь информативную ДНК: пятна или капли крови, слюны. Всё это началось ещё до эры метода ПЦР, для применения которого достаточно микроколичеств материала.
 Использование отпечатков пальцев для идентификации личности стало обыденностью в современной криминалистике
Фото: © Alisusha / Shutterstock / FOTODOM
Использование отпечатков пальцев для идентификации личности стало обыденностью в современной криминалистике
Фото: © Alisusha / Shutterstock / FOTODOM
— Но работу в этой области вы не продолжили. Почему?
— Криминалистика психологически очень сложная работа. Были и гражданские, и уголовные дела с тяжкими преступлениями, убийствами, маньяками, разными подробностями. Моя задача заключалась в том, чтобы оперативно научить специалистов пользоваться новым методом. Чтобы они как можно быстрее стали сами проводить такую экспертизу. В итоге этот метод революционизировал криминалистику.
— Вы много лет работаете — как в России, так и за рубежом. Расскажите о самых ценных для вас проектах.
— Тематика различна: эпигеномика, мозг, старение, гены болезней. В том числе сейчас в Сириусе мы занимаемся всеми этими направлениями. В каждом из них хотим найти что-то новое. Меня особенно интересует то, чего я не понимаю и о чём мало знаю.
Например, в лаборатории мы освоили культивирование и изучение медуз, хотя морской биологией раньше не занимались. Совместно с учёными из Университета Флориды опубликовали статью о ктенофорах, или гребневиках. Эти древние морские существа, возникшие примерно 500 млн лет назад, очень похожи на медуз, но относятся к другой группе живых организмов. Они привлекли особое внимание, когда появились в Азовском и Чёрном морях. Считается, что их завезли сюда из Америки на танкерах с балластной водой, которую те сбрасывали после заправки топливом. Эти существа в итоге съели местный зоопланктон. А потом случайно завезли другой подвид — и он уничтожил первых «пришельцев». Нас интересовало, были ли ктенофоры первыми, у кого появилась структура, которую можно назвать мини-мозгом.
 Ктенофора — морское животные, обитающие во всех частях Мирового океана, своим желеобразным полупрозрачным телом оно напоминает медузу
Фото: © goran_safarek / Shutterstock / FOTODOM
Ктенофора — морское животные, обитающие во всех частях Мирового океана, своим желеобразным полупрозрачным телом оно напоминает медузу
Фото: © goran_safarek / Shutterstock / FOTODOM
Мы расшифровали геном одного из видов гребневика и показали, что нервная система, по всей видимости, формировалась дважды в эволюции царства животных. Это было неожиданным открытием.
Более того, оказалось, что ктенофоры — древнейшие животные на Земле
Также мы выяснили, что у них нет микроРНК — коротких некодирующих молекул РНК, которые играют важную роль в контроле экспрессии генов. Раньше их находили у всех животных. Отсутствие этой системы указывает на уникальные особенности генетической регуляции гребневиков, что отличает их от других животных. Кстати, за открытие микроРНК Виктор Амброс, который сейчас работает в Университете Массачусетса, недавно получил Нобелевскую премию.
— К расшифровке генома человека вы тоже приложили руку?
— В 2022 году в журнале Science было опубликовано исследование, в числе авторов которого есть и мы, о расшифровке первого полного генома человека. В нём уже не было никаких непрочитанных дырок, которые особенно часто встречались в участках хромосом, которые называются центромерами. Необходимо было провести анализ очень специфических участков, которые состоят из множества тандемно повторяющихся последовательностей, поэтому их трудно было правильно выстроить в цепочку и секвенировать. Новые геномные технологии и биоинформатические подходы позволили заполнить все пробелы. Забавно, что к этой проблеме, по сути, относилась ещё моя дипломная работа, посвящённая первым секвенированным клонированным последовательностям таких центромерных повторов. В какой-то степени эта тема вернулась ко мне через много лет.
— Вы ещё занимаетесь исторической идентификацией — в частности, проводили анализ генетических материалов царской семьи Романовых…
— Мы сейчас активно развиваем область, которую называем исторической генетикой. И речь не только о конкретных личностях, но и о больших группах людей. Сейчас с помощью методов, которые раньше не применялись, можно реконструировать историю племён, народов, культур и отдельных индивидов, населявших территорию нашей страны в древности — буквально с палеолита и бронзового века до Средневековья.

Как историческая генетика раскрывает тайны прошлого
ЧитатьИсторическая генетика основана на конкретных данных, которые можно сопоставить с некой исторической информацией, документами. Например, мы занимались исследованием скифов. Геродот описывал их как воинственных степняков, которые вели полукочевой образ жизни, разводили скот и охотились. На основе ДНК мы можем сопоставлять их генетическое происхождение, направления миграции и другие факторы.
Сейчас заканчиваем научную статью по большому и важному для нашей страны исследованию, выполненному на основе анализа древней ДНК, о происхождении корней древнерусской общности.
— Расскажите ещё об исследовании процесса старения…
— На протяжении многих лет молекулярные генетики концентрировались на негативных аспектах старения: вредных мутациях и генетических факторах, приводящих к заболеваниям. А мы начали поиски того, что связано с благоприятными последствиями для здоровья и долголетия. То есть изучаем, кто и как может дожить до 100 лет, а также факторы, которые на это влияют.
Например, при болезни Альцгеймера наличие аллеля ApoE4 увеличивает риск развития заболевания в два-три раза. Но существуют и защитные мутации, снижающие вероятность возникновения недуга. Нашей задачей стало выявление подобных протекторов для возрастных патологий. Идеально было бы найти некие универсальные гены, обеспечивающие защиту от старения и ассоциированных с ним заболеваний. Чтобы подступиться к этой задаче, нужны какие-то модели. Например, люди, дожившие до 100 лет. Возможно, у них есть эти протектирующие генетические факторы, позволяющие прожить по крайней мере больше века.
 Ученые по всему миру пытаются разгадать тайну долголетия, изучая гены людей, доживших до 100 и более лет
Фото: © Rawpixel.com / Shutterstock / FOTODOM
Ученые по всему миру пытаются разгадать тайну долголетия, изучая гены людей, доживших до 100 и более лет
Фото: © Rawpixel.com / Shutterstock / FOTODOM
Ещё интересно понять, как молекулярные механизмы определяют ограничение в видовом долгожительстве. Например, человек доживает до максимального возраста — 114–116 лет. Больше люди не живут — это видовое ограничение. Что это за механизм, мы не знаем. Можем лишь строить гипотезы.
Ну и важно разобраться, как это всё изменить. Как повернуть старение вспять. Думаю, это возможно только через геномное репрограммирование. В связи с этим интересна модель обратного развития, которой мы сейчас занимаемся в нашей лаборатории. Речь идёт о медузе Turritopsis dorhnii, которую называют бессмертной. Жизнь животных линейна: рождение, созревание, размножение, старение (хотя этот пункт необязательный) и смерть. А этот маленький гидроидный организм, пройдя стадии от полипа до медузы, способен запустить программу вспять. Иначе говоря, на стадии медузы после некоторых изменений, которые мы назвали трансформизмом, животное превращается обратно в полип. Достигнув зрелости, оно способно вернуть свои клетки, образно выражаясь, в более юное состояние, соответствующее предыдущей стадии развития.
Мы смогли выловить Turritopsis d. в Адриатическом море, их помогли найти итальянские коллеги. Потом нам удалось культивировать этих животных в лабораторных условиях. Мы секвенировали их геном и продолжаем исследовать эпигентические механизмы, лежащие в основе этого уникального процесса, а также пытаемся определить ключевые молекулы, задействованные в нём.
 Адриатическое море — часть Средиземного моря между Апеннинским и Балканским полуостровами, омывает берега Италии, Словении, Хорватии, Боснии и Герцеговины, Черногории, Албании
Фото: © Balate.Dorin / Shutterstock / FOTODOM
Адриатическое море — часть Средиземного моря между Апеннинским и Балканским полуостровами, омывает берега Италии, Словении, Хорватии, Боснии и Герцеговины, Черногории, Албании
Фото: © Balate.Dorin / Shutterstock / FOTODOM
— Есть ли какие-то принципиальные различия между российской системой обучения молодых учёных и американской?
— В США студенты, как правило, платят за обучение, а не наоборот, как у нас. При этом не требуются, как в России, особые критерии для защиты диссертации у аспирантов — например, определённое число статей, импакт факторов. Решения просто принимает комитет, рассматривающий тезисы защищающегося.
— А как вы связали свою жизнь с Сириусом?
— Когда меня сюда пригласили, Университета «Сириус» ещё не было. Здесь шло обучение школьников, собранных со всех уголков страны, что само по себе было уникально. Мы общались с Еленой Владимировной Шмелёвой, и возникла идея создать полноценную научную генетическую лабораторию. Что довольно быстро и произошло.
Важно, что в университетской среде Сириуса, помимо прикладных тем, развивается фундаментальная наука. Именно благодаря ей появляются истинные инновации. Например, открытия в области генетики болезней Альцгеймера и Паркинсона позволили начать разработку лекарств. Аналогичным образом исследования в области исторической генетики открывают новые горизонты для понимания прошлого человечества.
— В чём для вас уникальность Сириуса?
— Сила Университета «Сириус» в том, что он привлекает ведущих специалистов со всей страны для реализации самых амбициозных исследовательских проектов. И многие выдающиеся учёные становятся частью местной академической среды.
 Евгений Рогаев со своей научной командой в Лабораторном комплексе университета «Сириус»
Фото: © Алёна Енченко / Медиадом «Сириус»
Евгений Рогаев со своей научной командой в Лабораторном комплексе университета «Сириус»
Фото: © Алёна Енченко / Медиадом «Сириус»
Ещё один важный момент — тесная связь со школьниками. Именно с раннего возраста нужно вовлекать молодёжь в науку. Уникальность возможностей Сириуса в том, что здесь организованы лабораторные занятия, где школьники принимают активное участие в исследованиях. Для них это особенная возможность совмещать учёбу и практическую работу в комфортных условиях. И пусть лично мне больше по душе именно научная экспериментальная деятельность, нежели чисто преподавательская, в Сириусе созданы отличные возможности обучать студентов на практике. Этот важный компонент надо внедрять в университетскую систему обучения и максимально его развивать.
Евгений Рогаев открыл и успешно реализует в Научно-технологическом университете «Сириус» уникальную программу магистратуры «Генетика и генетические технологии». Студенты на базе университета осваивают методы геномных исследований с использованием высокотехнологичного оборудования. С первых дней они вовлечены в передовые проекты Научного центра генетики и наук о жизни. Аспиранты направления «Генетика» под наставничеством Евгения Рогаева становятся младшими научными сотрудниками и участвуют в исследованиях мирового уровня.