Клетки-самоубийцы: зачем они нам?
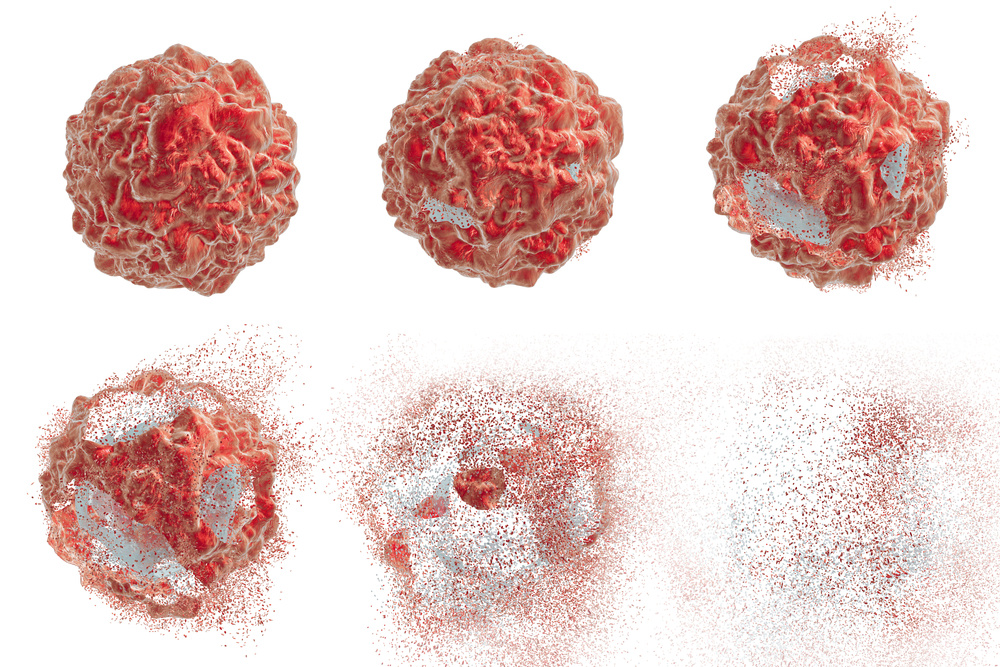
Расточительность нашего организма поразительна — каждый час в костном мозге и кишечнике умирают миллиарды клеток. Хотя у многих из них для этого нет причин — они здоровы и могут нормально выполнять свою работу. Так зачем же они это делают?
Клеточная смерть — обычное дело для нашего организма. Некоторые клетки нуждаются в обновлении, другие оказываются зараженными или перерождаются в раковые, поэтому должны самоликвидироваться. Клетки постоянно делятся, и смерть других помогает контролировать их количество в целом.
Часто запрограммированную гибель клеток называют апоптозом. И хотя это лишь одна из ее разновидностей, эти понятия уже стали синонимичными. Апоптоз можно назвать с самурайским законом биологии: лучше умереть, чем ошибиться. Согласно ему живая система включает механизмы самоликвидации, если не справляется со своей функцией и оказывается нежелательной для систем с более высоким положением в биологической иерархии.
Почему называется апоптозом?
Термин «апоптоз» был предложен в 1972 году американским исследователем Дж. Керром для описания программируемой гибели клетки. Слово это происходит от греческих слов «апо» — («завершенность») и «птоз» («падение») и может быть переведено как «опадание листьев». Суть термина подчеркивает его естественность, в отличие от некроза — смерти от повреждения. Проходит жизненный цикл — и падают плоды, опадают листья.
Апоптоз является защитным механизмом организма, он предотвращает развитие инфекции, образование генетически измененных клеток и тех, что создают токсичные для организма вещества. У него ключевая роль в иммунных процессах благодаря тому, что он обеспечивает гибель незрелых Т-лимфоцитов, реагирующих на «cвои» антигены. Проблемы с апоптозом ведут к развитию рака и аутоиммунных заболеваний. Ведь его функция — самоуничтожение мутировавших клеток. Клетка-мутант (не только раковая, хоть она и наиболее опасна, но и любая другая) распознается как чужеродная, и организм дает команду на ее самоуничтожение.
Механизм апоптоза только начинает изучаться, но фармакологи уже могут предложить свои эффективные лекарственные препараты, способные управлять этим процессом. И это, безусловно, достижение.
Сегодня насчитывается более 10 видов программируемой клеточной смерти, и, скорее всего, это не предел. Правда есть и такие клетки, которые не умирают. Например, клеточная линия HeLa, используемая в лабораториях по всему миру для экспериментов.
HeLa и бессмертная Генриетта Лакс
Молодая афроамериканка Генриетта Лакс умерла от осложнений рака шейки матки в 1951 году, но до сегодняшнего дня живет не только ее имя, но и частички тела. При жизни у нее с помощью биопсии взяли клетки эндотелия матки и отправили на обследование в больницу Johns Hopkins Hospital в Балтиморе, где руководитель лаборатории Джордж Гей обнаружил их удивительную особенность — они не погибали и могли делиться неограниченное число раз.
Так, Генриетта Лакс вошла в историю — ее именем назвали «бессмертные» клетки: Henrietta Lacks. За прошедшие десятилетия клетки ее организма неоднократно использовались для исследований рака, СПИДа и разработки вакцин.
Среди других вариантов запрограммированной гибели клеток можно выделить митоптоз — для митохондрий, органоптоз — для групп клеток и органов и феноптоз — для целого организма. А относительно недавно был открыт ферроптоз. Его подробно изучила команда международных ученых и отчиталась о результатах своей работы в журнале Current Biology. Выяснилось, что гибель клеток в этом случае запускается при участии железа и одновременного накопления липидов.
Что это знание дает в прикладном смысле? Подобные исследования помогают ученым лучше разобраться в процессе клеточной гибели и научиться его контролировать. Это пригодится в терапии многих заболеваний — например, нейродегенеративных или сердечно-сосудистых. А еще ферроптоз может быть связан с недостаточным ответом организма пациента на лучевую или химиотерапию.